
关于美柏
美柏医健(MyBioGate) 致力于链接中国与海外医健创新。美柏医健分享全球医健创新项目及前沿知识,提供中国资源与海外创新项目的高效对接服务,帮助中国投资者洞悉全球最新发展态势,帮助海外创新企业找到值得信赖的中国投资者和合作伙伴。
联系我们:info@mybiogate.com

微信扫一扫
关注公众号


2019-12-27
1.Qiagen拒绝收购要约,股价下跌

在过去一个月接触了多宗收购要约后,荷兰知名分子诊断开发商凯杰生物(Qiagen)最终决定单干,不过投资者并不高兴。
在凯杰表示将继续推进当前的业务计划后,凯杰的股价在圣诞节假期下跌了约25%。
今年10月,凯杰宣布与基因组学研究领域的技术与市场领导者Illumina建立为期15年的合作关系,不过并未选择进一步开发凯杰现有的二代测序(NGS)平台GeneReader,转而与Illumina合作开发基于NGS的体外诊断(IVD)产品以及相关硬件支持。这一消息是在凯杰未能实现第三季度目标以及长期担任首席执行官的Peer Schatz离职后发布的。
凯杰监事会主席Håkan Björklund表示,凯杰管理层认为其“正在进行的转型为股东和其他利益相关者创造未来价值提供了最佳策略”
11月中旬曾传言赛默飞世尔(Thermo Fisher Scientific)欲收购凯杰,目前凯杰已收到几份“有条件、无约束力的完全收购意向书”,目前凯杰市值达80亿美元。
凯杰的监督管理委员会表示,他们已经和潜在的收购者进行了几轮讨论,但发现他们“没有说服力”
Björklund在一份声明中说:“我们具备强大且差异化优势的分子检测解决方案组合,公司未来业绩有望显著增长。” 此次股价下跌使凯杰股价倒回31美元左右,接近赛默飞世尔提出收购要约之前的水平。
Qiagen与Illumina合作开发的NGS体外诊断(IVD)产品将覆盖多个疾病领域,包括基于Illumina的TruSight Oncology检测的肿瘤免疫(I/O)疗法伴随诊断分析,以及其他MiSeq Dx和NextSeq 550Dx系统的IVD。
2.绿叶制药新型抗抑郁药LY03005在美申报NDA

12月26日,绿叶制药集团宣布,其自主研发的新化合物——5-羟色胺-去甲肾上腺素-多巴胺三重再摄取抑制剂LY03005已正式向美国食品药品监督管理局(FDA)递交新药上市申请(NDA),用于治疗中重度抑郁症。LY03005也是绿叶制药在美国申报NDA的第二个中枢神经新药。
此次申报基于绿叶制药与美国FDA在EOP2-CMC会议(End-Of-Phase 2-CMC meeting)和PNDA会议(Pre-NDA meeting)上达成的共识。LY03005是基于绿叶制药的新型化合物(NCE/NTE)平台自主研发的中枢神经系统独家产品。LY03005是一种5-羟色胺-去甲肾上腺素-多巴胺三重再摄取抑制剂(SNDRI),其中的一个活性代谢产物是一种5-羟色胺-去甲肾上腺素双重再摄取抑制剂(SNRI)。
一般而言,传统抗抑郁药物,如选择性5-羟色胺再摄取抑制剂(SSRIs)、5-羟色胺-去甲肾上腺素再摄取抑制剂(SNRIs)存在快感缺乏、性功能障碍、无法改善认知障碍等药物缺陷,而5-羟色胺-去甲肾上腺素-多巴胺三重再摄取抑制剂(SNDRIs)预计将比传统药物更有助于保护患者的性功能、起效更快、疗效更好。
绿叶制药拥有涵盖LY03005化学成份、晶体形态及制剂的专利。化学成份及晶体形态的专利已在中国、美国、欧洲、日本及韩国等国家和地区获得。
绿叶制药集团管理层表示:“中枢神经治疗领域的全球患者人群庞大且不断增加,该类疾病无论对于患者还是对其家庭都造成了严重困扰。我们希望提供更多优质创新的原研药品,帮助全球更多有需要的患者,解决临床尚未满足的需求。”
* 关于抑郁症
抑郁症是中枢神经领域最常见的疾病之一,全球病患人数已超过3亿人。抑郁症是全球各地的首要致残原因,也是导致全球疾病负担的一个重大因素,目前只有不足一半的患者(在许多国家仅有不到10%的患者)接受有效治疗,病患形势严峻。
* 绿叶制药中枢神经领域管线布局
目前,绿叶制药正在加大投入力度推进中枢神经领域的新药开发。已有多个新药处于NDA或临床后期,预计将于2020年开始面向全球各主要医药市场陆续推出。除了LY03005之外,还有今年3月已在美国申报NDA的注射用利培酮缓释微球(LY03004)(治疗精神分裂症及双相情感障碍),目前其生产基地已通过美国FDA的上市批准前检查;此外还有LY03003(治疗帕金森病)、LY03010(治疗精神分裂症和分裂情感性障碍)、LY30410(治疗中轻度阿尔茨海默病)、LY03012(治疗慢性疼痛)等在研项目。
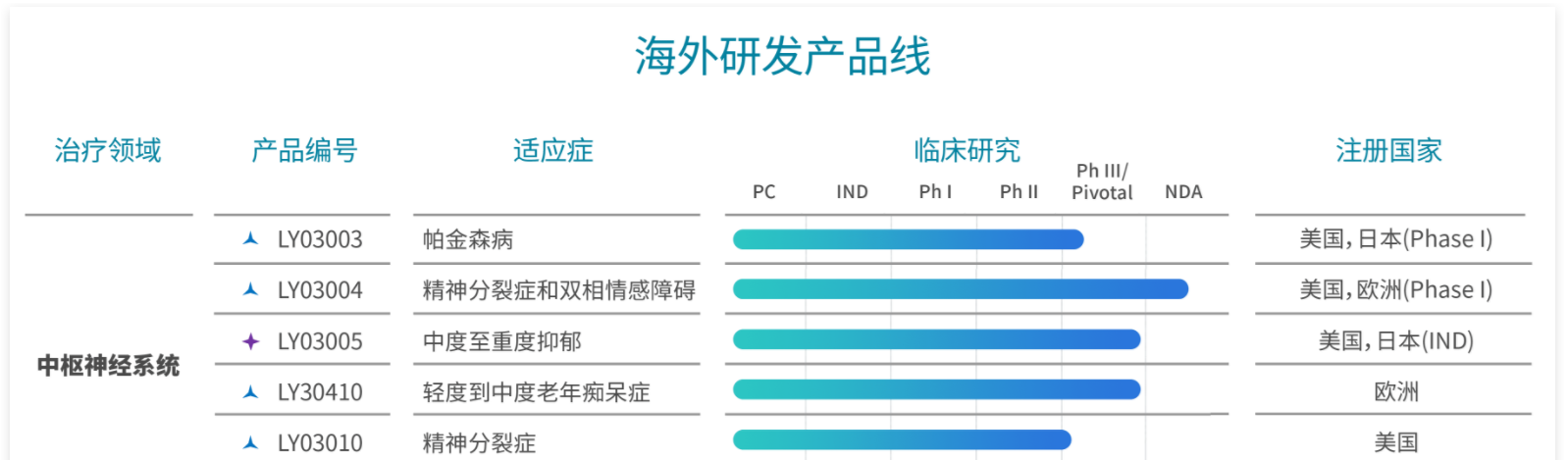
▲绿叶制药中枢神经领域海外研发产品线

▲绿叶制药中枢神经领域中国研发产品线
这些后续产品将通过绿叶制药目前覆盖的80多个国家和地区的市场渠道、全球化的供应链体系,与中枢神经领域的现有产品形成富有竞争力的产品组合,并进一步发挥协同效应,持续提升绿叶制药在该领域全球范围内的核心竞争力。
3.首批阿哌沙班仿制药获FDA批准,但可能要等到2026才能上市?
百时美施贵宝(BMS)/辉瑞的新型口服抗凝血剂(NOACs)艾乐妥(阿哌沙班)是全球最畅销的药物之一。GlobalData在今年11月发布的一份报告预测,到2025年,艾乐妥的全球销售额将达到187亿美元,成为仅次于默沙东Keytruda的全球第二大畅销药物。
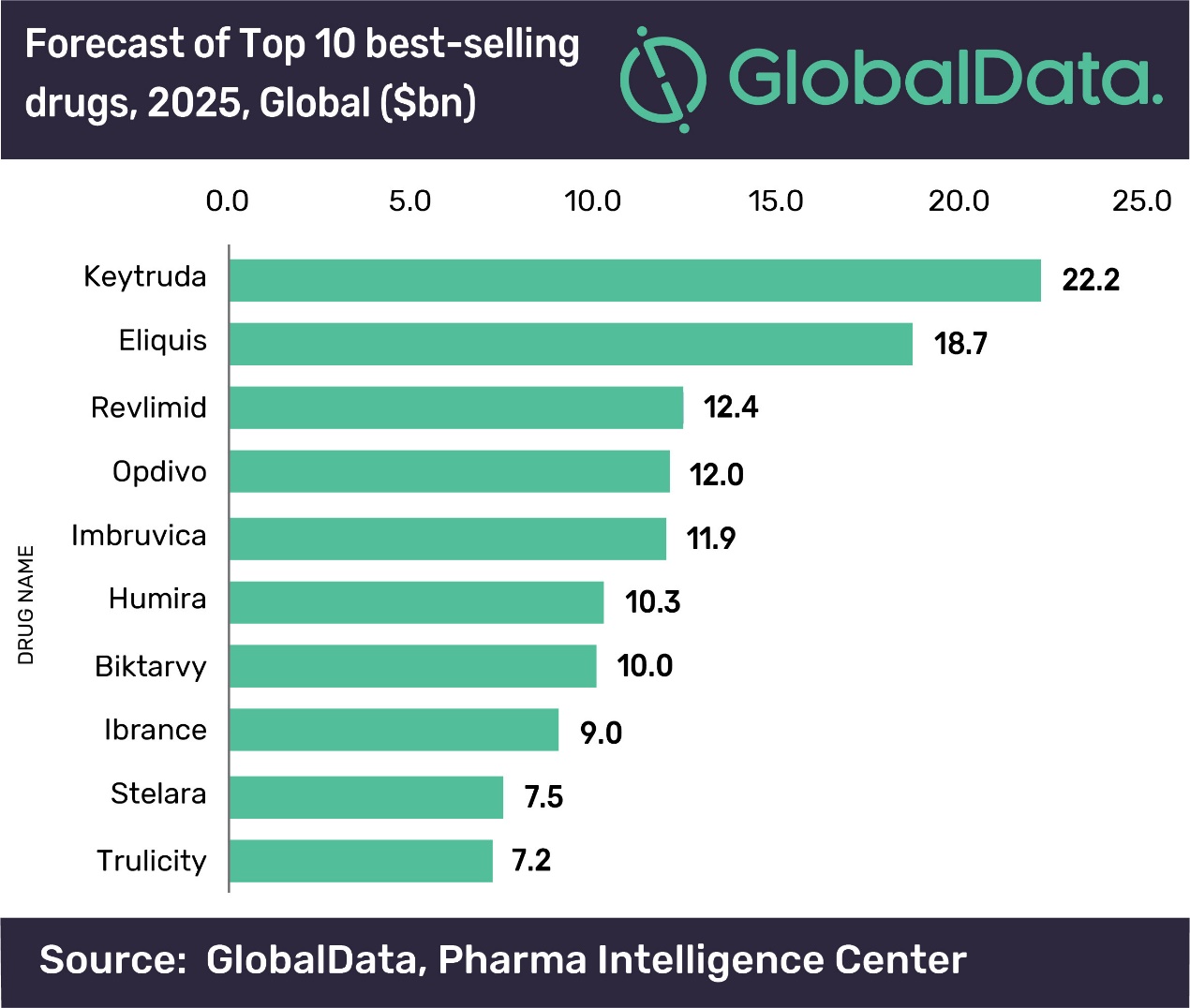
不过,阿哌沙班的仿制药威胁者一直虎视眈眈。
近日,FDA批准了由迈兰(Mylan)和Micro Labs生产的首批艾乐妥(阿哌沙班)仿制药。不过,尽管FDA近年来一直致力于通过促进仿制药上市来降低药价,阿哌沙班仿制药恐怕无法在短期内上市销售。
在一场正在进行的专利纠纷中,BMS正极力捍卫艾乐妥的专利期,不过这也难怪:
作为与新基合并前BMS最畅销的药物,甚至领先于PD-1抑制剂Opdivo,艾乐妥在2019年前三季度为BMS带来了59亿美元的收入。2019年前三季度,艾乐妥25%的同比增长率也远远超过了Opdivo的10%
至于辉瑞,艾乐妥在2019年前三季度总共为辉瑞带来了 31亿美元的收入,主要来自其盟友BMS的授权许可收入,但也有一部分是通过在较小市场的直接销售实现的。
2017年,25家仿制药公司表示已经向FDA递交阿哌沙班仿制药的上市申请。BMS/辉瑞很快竖起了专利高墙,对所有这些仿制药公司提起诉讼。
同年8月,美国专利和商标局(USPTO)授予艾乐妥一项关键的物质专利,将其从2023年2月延期至2026年11月。BMS/辉瑞辩称,在此之前阿哌沙班仿制药不可在美国上市。
据BMS最近递交的季度证券文件显示,虽然BMS/辉瑞已与几家不影响艾乐妥专利排他性的仿制药公司达成和解,但其他一些公司并未让步。
艾乐妥目前在新型口服抗凝血剂(NOACs)市场上处于领先地位,该领域竞品还包括强生/拜耳的拜瑞妥/Xarelto(利伐沙班)以及勃林格殷格翰的泰毕全/Pradaxa(达比加群酯)。
目前已经获得中国国家药品监督管理局(NMPA)批准的国产阿哌沙班制药商包括江苏豪森(2019-01-09)、正大天晴(2019-05-15)以及四川科伦(2019-11-04)。在原研药专利到期之前,目前还不能销售
拜瑞妥在2019年前三季度为拜耳带来了29.8亿欧元(合33.1亿美元)的收入,其中包括授权许可收入,同比增长了13%。强生仅在美国销售拜瑞妥,在2019年前三季度囊获了17亿美元的销售额,下降9%,可能与强生将精力放在努力使其纳入美国医疗保险(Medicare)覆盖有关。
尽管拜瑞妥第三季度在美国的销售额最终与去年相比持平,但与艾乐妥22%的全球增长率仍相去甚远。
根据EvaluatePharma 12月发布的2020年预测报告,艾乐妥位列第四大新销售增长点,预计2020年销售额将增长10.8亿美元。
+ 关注

hi,
提交评论




+ 关注
[Ta的贡献]
查看更多 >
投资人交流群
限量名额,微信扫码申请